
DES的出现为下肢动脉腔内治疗开辟了新的方向。选择适当的DES直径对于充分发挥其效用至关重要。过小的支架不足以支撑病变,而过大的支架则会刺激血管,导致过度内膜增生。目前,Eluvia支架是可用的DES之一,其最小支架外径为6mm。那么,它能否应用于直径为5mm的管腔呢?在选择DES规格时,应考虑哪些因素?如何平衡“牺牲”与收益?在2023年6月10日举行的第六届下肢动脉腔内治疗新技术峰会(LETS2023)上,复旦大学附属中山医院的蒋俊豪教授就DES直径选择的争议与考量进行了深入探讨。

考虑COF和RVD
慢性外扩力(COF)是指支架向外扩张时所产生的径向支撑力。若COF过高,则会引起内膜过度增殖,导致再狭窄。支架释放的程度与COF呈负相关,即释放越完全,COF越低。因此,支架直径与血管匹配至关重要,其中“如何定义参考血管直径(RVD)以及如何精准测量?”的重要性再度凸显。目前,许多血管外科专家都认为,RVD应选取血管中膜到中膜的距离(图1),并且依据后期随访影像显示支架后期处于中膜层。然而,这可能是由于支架缓慢扩张所致,也可能是支架直接扩张至中膜再由内膜向内生长的结果,目前尚未明确,值得深入探讨。
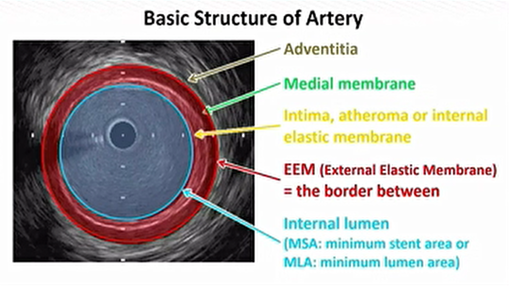
图1.动脉管腔结构。
根据现有下肢动脉腔内治疗相关研究,SFA直径约为5mm。然而,在超声影像中,我们能清楚地看到管腔中膜到中膜的距离与DSA上显示内膜到内膜的距离之间存在显著差异。日本血管外科专家Iida教授的研究表明,在IVUS影像下,血管直径(VD)显著高于DSA影像下(6.0±1.0mmvs.5.0±1.0mm,P<0.001);尤其在小血管中,这种差异更加显著(图2)。
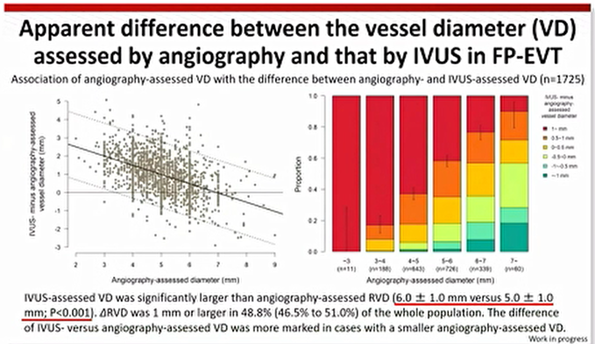
图2显示了IVUS与血管造影下管腔直径的差异。
S/V比值截断值。
S/V比值,即支架与血管的比值。2011年的一项研究表明,S/V比值是ISR相关预后的一个风险因素。该研究通过多变量COX回归分析发现,与再狭窄相关的预后风险因素包括支架断裂、CTO和S/V比值。此外,Kaplan-Meier分析显示,与S/V比值<1.30相比,S/V比值>1.30的一期通畅率显著降低(36%vs.73%,P=0.0005)。因此,S/V比值>1.30并不是一个好选择,但目前还没有明确的证据表明哪种S/V比值是最佳的。
在IMPERIAL临床研究的日本亚组中,Eluvia组共有56例患者,平均RVD为5.1±0.8mm。根据计算,S/V比值约为1.2。结果显示,Eluvia组1年一期通畅率为95.9%,2年为88.5%。这表明,当S/V比值=1.2时,可以获得不错的通畅性结果。
在2018年,有研究指出,腔内超声结果显示远段血管的管腔直径比病变段更大,且病变段的S/V比值也比远段更大(图3)。该研究结果表明,当使用病变部位的S/V比值时,当S/V≥1.2时,再狭窄风险比具有统计学意义(P=0.002),而远端健康部位的S/V比值与再狭窄风险并没有显著相关性。
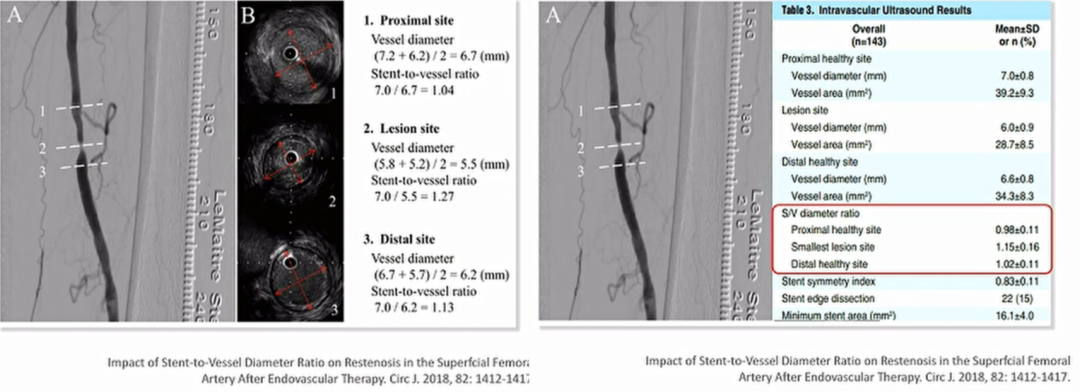
图3显示了近段、病变段和远段管腔尺寸的不一致性。
此外,即使支架和血管尺寸匹配,由于斑块的存在,病变段仍然存在COF。这解释了为什么ISR通常是随机的,而不是均匀的(见图4)。随着狭窄程度的增加,后续ISR的风险也越大。
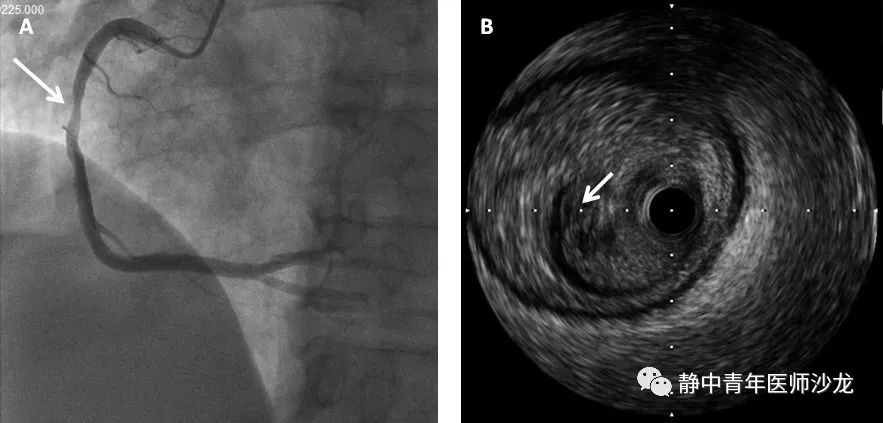
图4.管腔并非呈现均匀的形态。
DES与BMS的比较
自DES问世以来,关于“药物释放完全后,仅剩的BMS是否发生报复性再狭窄?”的问题一直存在争议。BATTLE试验对比了DES和BMS的疗效,结果显示在随访期间,DES组一期通畅率在初始阶段领先,但随后快速下降。在1年时,两组一期通畅率相差不大(图5)。EMINENT研究对比了Eluvia和BMS的疗效,其中DES组1年的一期通畅率高于BMS组。2年结果尚未公布。然而,CAPSICUM注册研究结果显示,在3年内ISR随时间递减,似乎没有报复性ISR(图6)。
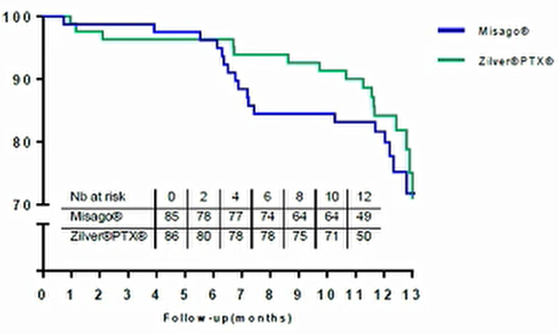
图5显示了DES与BMS一期通畅率的比较。
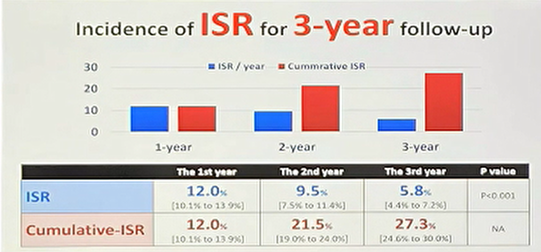
图6.注册研究结果显示,CAPSICUM具有显著的疗效。
与DCB+BMS相比。
专家提出,DES是带有药的BMS,那么能否用DCB+BMS来替换。以Eluvia和ZilverPTX这两款载药支架为例进行说明。这两款支架的载药方式不同,ZilverPTX的药物释放窗口期仅2个月,而Eluvia的药物释放覆盖了整个平滑肌细胞增殖期(图7)。因此,ZilverPTX不是严格意义上的药物洗脱支架,更应该是药物涂层支架,也更接近于DCB+BMS的治疗模式。IMPERIAL研究对比了Eluvia和ZilverPTX在SFA治疗中的疗效,术后1年,Eluvia组一期通畅率显著更高(92.1%vs.81.8%,P=0.0094);术后2年,Eluvia组也更高,但无统计学差异(83.0%vs.77.1%)。
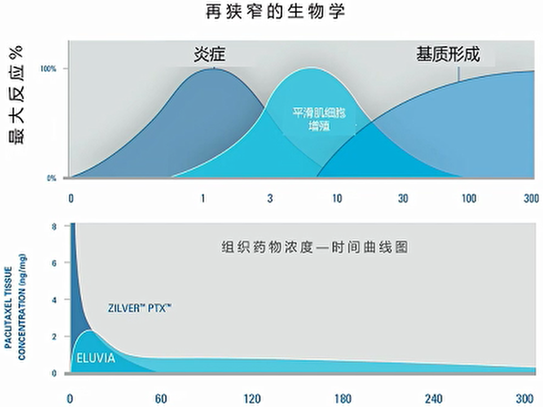
图7.再次狭窄的生物学和药物释放过程。
另外,从操作模式上看,与DES相比,无论是DCB+BMS,还是BMS+DCB,都存在一定的局限性。前者在处理不稳定斑块时,可能会在DCB阶段发生远端栓塞;而后者的BMS则会影响后续DCB药物的传递效率。因此,DES确实达到了1+1>2的效果。
总结:
总的来说,在选择DES直径时,首先应该准确测量RVD。根据S/V比值不超过1.2来进行选择。如果血管直径过小,没有S/V比值≤1.2的DES可供选择,那么临床医师需要考虑“COF提高带来的风险”与“DES带来的收益”。考虑到药物传递效率,对于血栓负荷较重的病变,不建议使用DCB。而对于需要长时间药物释放的病变位置,如股浅动脉开口处病变,建议使用DES。
本篇文章已获得专家和主办方的授权发布。
本文内容摘自《门诊》杂志的原创文章。
转载时,请务必获得授权并注明出处。

「Clinic门诊腔内血管|微信号:ClinicMZEndovascular」。这样可以吗?